Psicofarmacología de la esquizofrenia y de otros trastornos psicóticos
El de Psicosis es un término difícil de definir, y por tanto, frecuentemente se emplea de forma errónea, no solamente en los periódicos, el cine, la TV, sino también, por desgracia, entre los profesionales de la salud.
Descripción clínica de la psicosis
La psicosis es un síndrome (es decir, una mezcla de síntomas), que pueden asociarse a muchos trastornos psiquiátricos diferentes, pero que no constituye un trastorno específico por sí mismo en esquemas diagnósticos como el DSM-IV o ICD-10. Como mínimo, psicosis significa delirios y alucinaciones. También incluye generalmente síntomas como habla desorganizada y distorsiones groseras de la evaluación de la realidad.
Por lo tanto, se puede considerar la psicosis como un conjunto de síntomas en los que la capacidad mental de una persona, su respuesta afectiva y su capacidad para reconocer la realidad, para comunicarse y para relacionarse con otros están deterioradas. Los trastornos psicóticos tienen síntomas psicóticos como características definitorias, pero hay otros trastornos en los que los síntomas psicóticos pueden estar presentes, aunque sin ser necesarios para el diagnóstico.
Trastornos que requieren las presencia de psicosis:
Esquizofrenia
Trastornos psicóticos inducidos por sustancias (drogas)
Trastorno esquizofreniforme
Trastorno esquizoafectivo
Trastorno delirante
Trastorno psicótico breve
Trastorno psicótico compartido (o inducido)
Trastorno psicótico debido a una afección médica general
Trastornos que pueden estar o no asociados con síntomas psicóticos:
Manía
Depresión
Trastornos cognitivos
Demencia de Alzheimer
La psicosis en sí misma puede ser paranoide, desorganizada-excitada o depresiva. Las distorsiones perceptivas y las alteraciones motoras pueden estar asociadas a cualquier tipo de psicosis. Las distorsiones perceptivas incluyen estar desasosegado por voces alucinatorias; escuchar voces que acusan, culpan o amenazan con castigos; ver visiones; sufrir alucinaciones táctiles, gustativas u olfativas, o manifestar que las cosas y las personas familiares parecen cambiadas. Las alteraciones motoras consisten en posturas rígidas peculiares; signos manifiestos de tensión; muecas o risas inapropiadas; gestos repetitivos peculiares; hablar, refunfuñar o farfullar, o mirar alrededor como si oyesen voces.
Psicosis paranoide
Estos pacientes manifiestan:
Proyecciones paranoides, que incluye estar preocupado por creencias delirantes; creer que le persiguen a uno o conspiran contra él y creer que la gente o fuerzas externas controlan las propias acciones.
Beligerancia hostil es la expresión verbal de sentimientos de hostilidad, expresar irritabilidad y malhumor; tender a culpar a los demás de los problemas; expresar resentimiento, y quejarse y ponerle pegas a todo, así como manifestar recelo de la gente.
Expansividad grandiosa, que consiste en exhibir una actitud de superioridad; oír voces que alaban o ensalzan, y creer que uno tiene poderes extraordinarios, que es una personalidad muy conocida o que tiene una misión divina.
Psicosis desorganizada-excitada
Aquí lo que manifiestan los pacientes es:
Desorganización conceptual, caracterizada por dar respuestas irrelevantes o incoherentes; desviarse del tema; usar neologismos o repetir ciertas palabras o frases.
Desorientación, no saber dónde está uno, en qué estación del año, en qué año, o cuál es la propia edad.
Excitación, es la expresión de sentimientos sin restricción alguna; hablar apresuradamente; exhibir un estado de ánimo elevado o una actitud de superioridad; dramatizar sobre uno mismo o sobre los propios síntomas; hablar alto y alborotadamente, mostrar hiperactividad e intranquilidad y hablar en exceso.
Psicosis depresiva
Se caracteriza por retardo, apatía y un sentimiento ansioso de castigo de uno mismo y de culpa.
El retardo y la apatía se manifiestan por hablar lentamente; indiferencia ante el propio futuro; expresión facial fija; lentitud de movimientos; déficit de la memoria reciente, bloqueo del habla; apatía hacia uno mismo o hacia los propios problemas; apariencia descuidada; hablar bajo cuchicheos, y no contestar a las preguntas.
El sentimiento ansioso de castigo de uno mismo y de culpa consiste en una tendencia a culparse o condenarse a uno mismo; ansiedad sobre temas específicos; aprensión acerca de vagos acontecimientos del futuro; una actitud de desprecio hacia uno mismo; un estado de ánimo deprimido; sentimientos de culpabilidad y remordimiento, preocuparse por pensamientos suicidas, ideas no deseadas y miedos específicos, y sentirse indigno o pecador.
Cinco dimensiones sintomáticas de la exquizofrenia
Aunque la esquizofrenia es quizá el tipo más común y mejor conocido de enfermedad psicótica, ésta no es sinónimo de psicosis, sino una de las muchas causas de psicosis. Afecta al 1% de la población, aproximadamente.
La esquizofrenia es un trastorno que debe durar seis meses o más, incluyendo al menos un mes de delirios, alucinaciones, habla desorganizada, conducta enormemente desorganizada o catatónica, o síntomas negativos.
Los delirios suelen implicar una interpretación errónea de las percepciones o de las experiencias. El tipo de delirio más habitual es el persecutorio, pero pueden incluir otros temas como el referencial, somático, religioso o el de grandeza.
Las alucinaciones pueden ocurrir en cualquier modalidad sensorial (auditiva, visual, olfatoria, gustativa y táctil), aunque las más comunes son las auditivas.
Numerosos estudios clasifican los síntomas de esta enfermedad en cinco dimensiones: síntomas positivos, síntomas negativos, síntomas cognitivos, síntomas agresivos / hostiles y síntomas depresivos / ansiosos.
Varias enfermedades comparten, además de la esquizofrenia, estas dimensiones sintomáticas.
Síntomas positivos
Los síntomas positivos parecen reflejar un exceso de las funciones normales y típicamente incluyen los siguientes síntomas:
Delirios
Alucinaciones
Distorsiones o exageraciones en el lenguaje y la comunicación
Habla desorganizada
Conducta desorganizada
Conducta catatónica
Agitación
Los trastornos, aparte de la esquizofrenia, que pueden tener síntomas positivos incluyen el trastorno bipolar, el trastorno esquizoafectivo, la depresión psicótica, la enfermedad de Alzheimer y otras demencias orgánicas, las enfermedades psicóticas infantiles, la psicosis inducida por drogas y otras.
Síntomas negativos
Los síntomas negativos incluyen al menos cinco tipos de síntomas (que comienzan todos con la letra a):
Afectividad embotada, consistente en limitaciones en el rango e intensidad de la expresión emocional.
Alogia, que consiste en restricciones en la fluidez y productividad del pensamiento y el habla.
Abulia, consistente en limitaciones en la iniciación de conductas dirigidas a una meta.
Anhedonia, es decir, falta de placer.
Atención deteriorada.
Síntomas debidos a la reducción de las funciones normales:
Afectividad embotada
Retraimiento emocional
Escasa capacidad de contacto
Pasividad
Retraimiento social apático
Asociados a largos períodos de hospitalización y a un pobre funcionamiento social:
Dificultad de pensamiento abstracto
Pensamiento estereotipado
Falta de espontaneidad
Alogia
Abulia
Anhedonia
Atención deteriorada
A su vez, pueden ser:
Primarios: los que constituyen el núcleo de los déficit primarios de la propia esquizofrenia.
Secundarios: los asociados a la depresión, síntomas extrapiramidales (SEP), síntomas asociados a la privación ambiental y secundarios a los síntomas positivos.
Síntomas cognitivos
Las deficiencias cognitivas más comunes y más graves de la esquizofrenia pueden incluir el deterioro de la fluidez verbal (capacidad de producir habla espontánea, uso extraño del lenguaje, incluyendo incoherencia, asociaciones imprecisas y neologismos), los problemas con el aprendizaje en serie y el deterioro de la vigilancia de la función ejecutiva (atención deteriorada: problemas para mantener y centrar la atención, concentrarse; procesamiento de la información deficiente: establecer prioridades y modular la conducta en base a señales sociales).
Los síntomas cognitivos no sólo están asociados a la esquizofrenia, sino también a varios trastornos como el autismo, la enfermedad de Alzheimer y las afecciones derivadas de un accidente cerebrovascular (postapoplejías).
Síntomas agresivos y hostiles
Pueden coincidir en parte con los síntomas positivos, pero específicamente acentúan los problemas de control de impulsos.
Entre ellos se encuentran: la hostilidad manifiesta, como el maltrato verbal o físico, o incluso el ataque; comportamientos orientados a autolesionarse, incluyendo el suicidio y el incendio provocado u otros daños a la propiedad; la falta de contención sexual.
Estos síntomas también están asociados al trastorno bipolar, la psicosis infantil, trastorno borderline, abuso de drogas, TDA-H, trastornos conductuales en niños, etc.
Síntomas depresivos y ansiosos
Los síntomas depresivos y ansiosos se asocian frecuentemente a la esquizofrenia, pero eso no significa necesariamente que cumplan los criterios de diagnósticos para un trastorno de ansiedad o depresión comórbido. Sin embargo, el estado de ánimo deprimido y ansioso, la culpa, la tensión, la irritabilidad y la preocupación suelen acompañar a la esquizofrenia.
También acompañan a otros trastornos psiquiátricos como el trastorno bipolar, la depresión mayor, trastorno esquizoafectivo, causas orgánicas de la depresión, abuso de sustancias, etc.
Las 4 vías dopaminérgicas clave y la base biológica de la esquizofrenia
La base biológica de la esquizofrenia sigue siendo desconocida. Sin embargo, el neurotransmisor monoaminérgico dopamina ha desempeñado un papel clave en diversas hipótesis.
Hay cuatro vías dopaminérgicas bien definidas en el cerebro:
la vía dopaminérgica mesolímbica
la vía dopaminérgica mesocortical
la vía dopaminérgica nigroestriada
la vía dopaminérgica tuberoinfundibular
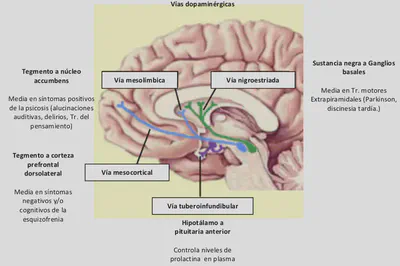
La vía dopaminérgica mesolímbica
Se proyecta desde los cuerpos celulares dopaminérgicos del área tegmental ventral del tronco cerebral a los terminales axónicos de las áreas límbicas del cerebro, como el nucleus acumbens, una parte del cerebro que parece estar implicada en muchas conductas emocionales de la psicosis. Se cree que la hiperactividad de las neuronas dopaminérgicas de esta vía desempeña un importante papel en las sensaciones placenteras, la potente euforia de las drogas de abuso, delirios y alucinaciones (especialmente auditivas) y trastornos del pensamiento.
Las observaciones de que las sustancias que aumentan o disminuyen la dopamina, aumentan o reducen los síntomas positivos de la esquizofrenia, han llevado a formular la hipótesis dopaminérgica de los síntomas positivos, ya que explica los síntomas psicóticos positivos tanto si forman parte de la enfermedad de la esquizofrenia o de una psicosis inducida por drogas como si los síntomas acompañan a la manía, la depresión o la demencia. Esta hiperactividad de las neuronas dopaminérgicas mesolímbicas puede desempeñar también un papel en los síntomas agresivos y hostiles de esta enfermedad u otras relacionadas.
La vía dopaminérgica mesocortical
Esta vía está relacionada con la anterior y se proyecta desde el área tegmental del mesencéfalo, pero envía sus axones a la corteza límbica, donde es posible que éstos desempeñen un papel en la mediación de los síntomas negativos y cognitivos de la esquizofrenia. Algunos investigadores creen que estos síntomas pueden deberse a un déficit de dopamina en las áreas de proyección mesocorticales, como la corteza prefrontal dorsolateral y un proceso neurodegenerativo en curso de la vía dopaminérgica mesocortical podría explicar un progresivo empeoramiento de los síntomas.
Así pues, esto plantea un dilema terapéutico: ¿cómo se puede incrementar la dopamina en la vía mesocortical al mismo tiempo que se reduce la actividad dopaminérgica en la vía mesolímbica?
La vía dopaminérgica nigroestriada
Se proyecta desde los cuerpos celulares dopaminérgicos de la sustancia negra a través de axones que terminan en los ganglios basales o estriados. Forma parte del sistema nervioso extrapiramidal. Las deficiencias dopaminérgicas en esta vía causan trastornos motores, pudiendo causar parkinsonismo, con temblor, rigidez, acinesia (falta de movimiento), discinesia (lentitud del movimiento), acatisia (un tipo de desasosiego) y distonía (movimientos de torsión especialmente en la cara y cuello). La hiperactividad de la dopamina en esta vía constituye la base de varios trastornos motores hipercinéticos como la corea, las discinesias y discinesias tardías inducidas por neurolépticos (bloqueando el receptores D2), y tics.
La vía dopaminérgica tuberoinfundibular
Las neuronas dopaminérgicas de esta vía se proyectan desde el hipotálamo a la pituitaria anterior. Su actividad está dirigida a inhibir la liberación de prolactina (hormona que produce la secreción de leche). Si el funcionamiento de estas neuronas se ve interrumpido por una lesión o la acción de determinadas sustancias, se elevarán los niveles de prolactina con el consiguiente aumento de secreción de leche (galactorrea), amenorrea y posiblemente otros problemas, como disfunciones sexuales.
Hipótesis neuroevolutiva de la esquizofrenia
Una hipótesis sobre la etiología de la esquizofrenia se refiere a las anomalías en el desarrollo cerebral fetal durante las primeras etapas de la selección y la migración neuronales, que no se manifiestan hasta la adolescencia.
Otros datos sugieren que una ofensa al cerebro (infecciones víricas hasta inanición, pasando por procesos autoinmunes y otros problemas padecidos por la madre embarazada) en las primeras fases del desarrollo fetal podría contribuir a causar la esquizofrenia.
En cuanto a las bases genéticas de la esquizofrenia parece estar clara la implicación de múltiples anomalías, cada una de las cuales contribuya de forma compleja a la vulnerabilidad a la esquizofrenia, y que probablemente no se manifiesten en una enfermedad psicótica si no se presentan otros factores ambientales críticos.
Hipótesis neurodegenerativa de la esquizofrenia
La presencia de anomalías tanto funcionales como estructurales mostrada en estudios de neuroimagen del cerebro de pacientes esquizofrénicos, sugiere que durante la evolución de la enfermedad puede existir un proceso neurodegenerativo con pérdida progresiva de función neuronal. La evolución progresiva de esta enfermedad y los cambios en las respuesta de los pacientes a los tratamientos también lo sugieren.
La esquizofrenia progresa de un estado en gran medida asintomático anterior a la adolescencia, a un estado prodromal de “excentricidad” e inicio de síntomas negativos sutiles alrededor de los veinte años de edad. Se distinguen cuatro fases:
Etapa I: paciente funcional al 100% y prácticamente asintomático.
Etapa II: fase prodromal, conductas extrañas y síntomas negativos sutiles.
Etapa III: fase aguda, que suele anunciarse bastante dramáticamente alrededor de los veinte años y continúa hasta los cuarenta años aprox., con síntomas positivos destructivos, remisiones y caídas, pero sin recuperar del todo los niveles previos de funcionamiento. Este suele ser un estado caótico de la enfermedad, con una evolución descendente progresiva.
Etapa IV: denominada, a veces, agotamiento, entre los cuarenta y cincuenta años, con síntomas negativos y cognitivos prominentes, con algunos altibajos, pero con un considerable descenso del nivel de funcionamiento basal.
El hecho de que un paciente puede responder menos a un tratamiento antipsicótico durante sucesivos episodios o exacerbaciones sugiere que la esquizofrenia es “peligrosa para el cerebro”.
Excitotoxicidad
Una importante idea propuesta para explicar el curso descendente de la esquizofrenia y el desarrollo de resistencia al tratamiento es la de que en esta enfermedad los acontecimientos neurodegenerativos pueden estar mediados por un tipo de acción excesiva del neurotransmisor glutamato, que ha pasado a conocerse como excitotoxicidad.
Esta hipótesis propone que las neuronas degeneran debido a la excesiva neurotransmisión excitadora en las neuronas glutamatérgicas.
También se ha propuesto como explicación para la neurodegeneración en diversas patologías como el Alzheimer, Parkinson, ELA (esclerosis lateral amiotrófica o enfermedad de Lou Gehrig) e incluso la apoplejía.
Neurotransmisión glutamatérgica
La síntesis del glutamato: El aminoácido glutamato, o ácido glutámico, es un neurotransmisor, aunque su función predominante es la de servir como aminoácido esencial en la biosíntesis de proteínas. Se produce a partir de la glutamina por la acción del enzima glutaminasa. Las células gliales adyacentes a las neuronas glutamatérgicas también proporcionan glutamina de sus reservorios por medio del enzima glutamín-sintetasa que convierte el glutamato en glutamina.
La eliminación del glutamato se produce por la mediación de una bomba de transporte presináptico y otra situada en la glía.
Entre los receptores del glutamato están los que se encuentran unidos a un canal iónico, el NMDA (N- metil-D-aspartato), el AMPA y el kainato. Y el receptor metabotrópico que pertenece a la superfamilia de receptores ligados a la proteína G.
En este análisis destacaremos el receptor NMDA, que tiene un canal de calcio y múltiples receptores alrededor de este canal que actúan conjuntamente como moduladores alostéricos. Uno para la glicina, otro para las poliaminas, otro para el zinc, otro para el magnesio que bloquea el canal iónico y otro para el inhibidor PCP.
En la excitotoxicidad y el sistema glutamatérgico en enfermedades neurodegenerativas como la esquizofrenia tomamos como mediador al receptor NMDA que en su proceso normal de neurotransmisión excitadora se desboca y la neurona es literalmente excitada hasta la muerte. El mecanismo se inicia con una actividad glutamatérgica temeraria. Esto podría causar una peligrosa apertura del canal de calcio debido a que, si entra demasiado calcio en la célula a través de los canales abiertos, éste envenenaría la célula activando los enzimas intracelulares que forman radicales libres potencialmente peligrosos.
Métodos terapéuticos experimentales
Bloqueo de la neurodegeneración y la apoptosis: antagonistas del glutamato, “barrenderos” de radicales libres e inhibidores de la caspasa
Se están desarrollando varios métodos terapéuticos basados en el glutamato, la excitotoxicidad y los radicales libres.
Posiblemente los antagonistas del glutamato puedan ser neuroprotectores. Los barrenderos de radicales libres, son fármacos que tienen la propiedad química de absorber y eliminar dichos radicales. Uno de estos barrenderos débiles, que ya se ha evaluado en la enfermedad de Parkinson y en la discinesia tardía, es la vitamina E. Los lazaroides, son fármacos más poderosos y tienen la propiedad de rescatar de la muerte a las neuronas que degeneran. Otros fármacos bloquean los enzimas caspasa, pues se piensa que este sistema enzimático es necesario para que se produzca la apoptosis.
Tratamiento presintomático
Esta estrategia provocando debate e incluso polémica, ya que en una fase temprana el diagnóstico de la esquizofrenia no es preciso y no hay ninguna garantía. Sin embargo, es evidente que en los pacientes que están menos tiempo enfermos antes de iniciar el tratamiento con fármacos antipsicóticos la probabilidad de que respondan a ellos es mayor que en aquellos otros en los que la enfermedad ha permanecido más tiempo antes del tratamiento. Hay investigadores que están ampliando estas ideas en parientes de primer grado, prácticamente asintomáticos, de personas en cuyas familias hay numerosos pacientes esquizofrénicos.
Hipótesis mixta neuroevolutiva/neurodegenerativa
Es posible que la esquizofrenia sea un proceso degenerativo superpuesto a una anomalía neuroevolutiva.
Los lugares donde se podría encontrar la degeneración están en las neuronas dopaminérgicas que se proyectan a la corteza y las proyecciones glutamatérgicas que vuelven de la corteza a las estructuras subcorticales. Incluso es posible que se de la excitotoxicidad en dichas estructuras cuando se producen los síntomas positivos durante las recaídas psicóticas.
Agentes antipsicóticos
Las características específicas de los tratamientos antipsicóticos diferirán, por supuesto, en función de cuál sea el trastorno psicótico (es decir, esquizofrenia u otro), y de cómo haya respondido el paciente a los tratamientos en el pasado. Por desgracia, también las consideraciones económicas constituyen otro factor, ya que los nuevos fármacos resultan bastante caros, si bien, por fortuna, también pueden reducir el coste global del tratamiento.
Fármacos psicóticos convencionales
Los primeros fármacos antipsicóticos se dieron en llamar neurolépticos y surgieron de observaciones clínicas causales, como la clorpromacina (un antihistamínico). La capacidad de estos fármacos de producir en animales de laboratorio neurolepsis (extrema lentitud o ausencia de movimientos motores) fue la principal causa de su descubrimiento y debido a esto se les denomina neurolépticos. Estos fármacos antipsicóticos originarios (convencionales) causan también un equivalente humano de la neurolepsis, caracterizado por retardo psicomotor, sosiego emocional e indiferencia afectiva.
El bloqueo de los receptores dopaminérgicos D2 como mecanismo de acción de los antipsicóticos convencionales
A finales de la década de los 60 y principios de la de los 70 se reconoció ampliamente que la propiedad farmacológica clave de todos los neurolépticos con propiedades antipsicóticas era su capacidad para bloquear los receptores dopaminérgicos. Esta acción ha resultado ser la responsable no sólo de la eficacia antipsicótica de los fármacos antipsicóticos convencionales, sino también de la mayoría de sus efectos secundarios indeseables, incluyendo la neurolepsis.
Las acciones terapéuticas de los fármacos antipsicóticos convencionales se deben al bloqueo de los receptores D2 específicamente en la vía dopaminérgica mesolímbica. Esto tiene el efecto de reducir la hiperactividad en esta vía, que según se cree, causa los síntomas positivos de la psicosis. Por desgracia, con los antipsicóticos convencionales no es posible bloquear sólo los receptores D2 en la vía dopaminérgica, ya que, tras su ingestión oral, dichos fármacos se reparten por todo el cerebro buscando los receptores D2 y los bloquean en todas las vías. Esto hace que el bloqueo de los receptores D2 mesolímbicos tenga un elevado precio. Concretamente:
Vía dopaminérgica mesocortical, donde es posible que la dopamina sea ya insuficiente, puede causar síntomas negativos y cognitivos, o empeorarlos (síndrome deficitario inducido por neurolépticos)
Vía dopaminérgica nigroestriada, produce trastornos motores parecidos a la enfermedad de Parkinson, llamados parkinsonismo inducido por fármacos o síntomas extrapiramidales (SEP). Y lo que es peor, si se bloquean de forma crónica, pueden producir un trastorno motor hipercinético llamado discinesia tardía (movimientos faciales y linguales como masticación constante, protrusiones de la lengua y muecas faciales, así como movimientos de las extremidades rápidos, espasmódicos o coreiformes). Puede ser irreversible, aunque se retire el tratamiento con estos fármacos.
Vía tuberoinfundibular, al bloquearse los receptores D2 hace que aumenten las concentraciones de prolactina en plasma, afección llamada hiperprolactinemia, asociada a la galactorrea (secreciones mamarias) y amenorrea (períodos menstruales irregulares). La hiperprolactinemia puede interferir en la fertilidad (especialmente de las mujeres) y desmineralización de los huesos más rápidamente en mujeres postmenopáusicas que no hayan sido tratadas con terapia de sustitución de estrógenos. Otros posibles problemas asociados al aumento de prolactina son disfunción sexual y aumento de peso.
El dilema del bloqueo de los receptores dopaminérgicos D2 en la cuatro vías dopaminérgicas
¿Qué se debe hacer si se desea reducir la dopamina en las vías dopaminérgicas mesolímbicas con el fin de tratar los síntomas psicóticos positivos, que teóricamente están mediados por neuronas dopaminérgicas mesolímbicas hiperactivas, y, sin embargo, al mismo tiempo aumentar la dopamina en la vía dopaminérgica mesocortical para tratar los síntomas negativos y cognitivos, mientras se mantiene el tono dopaminérgico inalterado tanto en la vía dopaminérgica nigroestriada como en la tuberoinfundibular para evitar efectos secundarios? Este dilema parece parcialmente resuelto con los antipsicóticos atípicos.
Riesgos y beneficios del tratamiento a largo plazo con antipsicóticos convencionales
Teniendo en cuenta que la interrupción del tratamiento tras la reducción de los síntomas psicóticos positivos produce un elevado número de recaídas, los pacientes dudan que los beneficios del tratamiento a largo plazo compense los efectos secundarios, de manera que con demasiada frecuencia los pacientes prefieren el riesgo de recaer antes que los efectos secundarios subjetivamente inaceptables de los antipsicóticos convencionales, llevándoles a interrumpir el tratamiento, a no cumplir las prescripciones, a recaer y a llevar una vida tipo “puerta giratoria” (entrando y saliendo del hospital).
Especialmente inaceptables para los pacientes son la inquietud motora y los SEP como la acatisia, la rigidez y el temblor, así como el embotamiento cognitivo y el retraimiento social, la anhedonia y la apatía.
Existe incluso la posibilidad de una rara –aunque potencialmente fatal- complicación llamada síndrome neuroléptico maligno, que se asocia a una rigidez muscular extrema, fiebre alta, coma e, incluso, la muerte.
Propiedades convencionales bloqueantes colinérgicas muscarínicas de los antipsicóticos
Una acción farmacológica particularmente importante de algunos antipsicóticos convencionales es su capacidad de bloquear los receptores colinérgicos muscarínicos. Esto puede causar efectos secundarios indeseables como sequedad de boca, visión borrosa, estreñimiento y embotamiento cognitivo. Por otra parte, los antipsicóticos convencionales que causan más SEP tienen propiedades anticolinérgicas débiles, mientras que los que causan menos SEP son los agentes que poseen propiedades anticolinérgicas más fuertes.
¿Y cómo puede el bloqueo de los receptores colinérgicos muscarínicos reducir los SEP causados por el bloqueo de los receptores dopaminérgicos D2 en la vía nigroestriada? La razón parece ser que la dopamina y la acetilcolina ejercen una relación recíproca en la vía nigroestriada.
Normalmente la dopamina inhibe la liberación de acetilcolina de las neuronas colinérgicas nigroestriadas postsinápticas, suprimiendo así la actividad de la acetilcolina en esa zona. Si la dopamina ya no puede suprimir la liberación de acetilcolina debido a que los receptores dopaminérgicos están bloqueados por un fármaco antipsicótico convencional, entonces la acetilcolina se vuelve demasiado activa.
Una forma de compensar esta hiperactividad de la acetilcolina es bloqueándola con un agente anticolinérgico, y, si las propiedades anticolinérgicas están presentes en el mismo fármaco con propiedades bloqueantes D2, éstas tenderán a mitigar los efectos del bloqueo D2 en la vía dopaminérgica negroestriada. Así, los antipsicóticos convencionales con propiedades anticolinérgicas potentes tienen menos SEP que los antipsicóticos convencionales con propiedades anticolnérgicas débiles.
Por desgracia, este uso concomitante de agentes anticolinérgicos no reduce la capacidad de los antipsicóticos convencionales de causar discinesia tardía. Asimismo, causa los conocidos efectos secundarios asociados a los agentes antipsicóticos, como sequedad en la boca, visión borrosa, estreñimiento, retención de orina y disfunción cognitiva.
Otras propiedades farmacológicas de los agentes antipsicóticos convencionales
Hay todavía otras acciones farmacológicas asociadas a los fármacos antipsicóticos convencionales. Éstas incluyen actividad no deseada en los distintos receptores:
H1: ganancia de peso y somnolencia
Alfa 1: disminución de la presión arterial (hipotensión ortostática), mareo y somnolencia
Receptores colinérgicos muscarínicos: sequedad de boca, visión borrosa, estreñimiento, retención de orina y disfunción cognitiva.
Estos agentes difieren en estas propiedades causando más o menos efectos secundarios.
Fármacos antipsicóticos: el antagonismo serotoninérgico-dopaminérgico y lo que varios fármacos antipsicóticos tienen en común
¿Qué es un antipsicótico atípico? Desde una perspectiva farmacológica se pueden definir como antagonistas serotoninérgicos-dopaminérgicos (ASD). Así pues, es muy importante comprender las interacciones serotonina-dopamina en cada una de las cuatro vías dopaminérgicas.
Desde una perspectiva clínica son atípicos por sus reducidos síntomas extrapiramidales y su eficacia en los efectos negativos de la psicosis, además de los positivos.
Los antipsicóticos atípicos también poseen características que los distinguen entre sí.
El antagonismo serotoninérgico-dopaminérgico y el control serotoninérgico de la liberación de dopamina en las 4 vías dopaminérgicas clave
La serotonina inhibe la liberación de la dopamina de los terminales axónicos dopaminérgicos en las diversas vías dopaminérgicas, pero el grado de control difiere de una vía dopaminérgica a otra.
Interacciones serotonina-dopamina en la vía nigroestriada
Las neuronas serotoninérgicas del rafe del tronco cerebral inervan a los cuerpos celulares dopaminérgicos de la sustancia negra y también se proyectan a los ganglios basales, donde los terminales axónicos serotoninérgicos se hallan muy próximos a los terminales axónicos dopaminérgicos. En ambas áreas, la serotonina interactúa con los receptores 5HT2A postsinápticos de la neurona dopaminérgica, y esto inhibe la liberación de dopamina.
Este fuerte control sobre la liberación de dopamina se da en dos niveles:
En el nivel de la inervación serotoninérgica de la sustancia negra, los terminales axónicos llegan de la sinapsis del rafe con los cuerpos celulares y las dendritas de la células dopaminérgicas.
En el nivel de los terminales axónicos, sin embargo, la interacción serotoninérgica con las neuronas dopaminérgicas puede darse a través de las sinapsis axoaxónicas o a través de la neurotransmisión por volumen (no sináptica) de la serotonina, que se difunde a los terminales axónicos dopaminérgicos desde los terminales axónicos serotoninérgicos cercanos, pero sin sinapsis alguna.
La vía nigroestriada y la farmacología de síntomas extrapiramidales reducidos
Afortunadamente el antagonismo 5HT2A revierte el antagonismo D2 en la vía dopaminérgica nigroestriada.
Dado que la estimulación de los receptores 5HT2A inhibe la liberación de dopamina, tendría sentido que lo contrario también fuera cierto. Y, en realidad, ese es el caso.
Cuando la liberación de dopamina resulta potenciada por un antipsicótico atípico a través de los receptores 5HT2A, esto permite que la dopamina extra compita con el antipsicótico atípico para revertir el bloqueo de los receptores D2. No es extraño que esto dé como resultado la reducción o, incluso, la ausencia de SEP y de discinesia tardía, dado que existe una reducción del bloqueo de los receptores D2 en esta vía.
Las propiedades antagonistas serotoninérgicas-dopaminérgicas (ASD) de todos los antipsicóticos atípicos explotan esa capacidad del antagonismo 5HT2A de desempeñar el papel de una especie de “tira y afloja” en relación al antagonismo D2, causando la liberación de dopamina, que a su vez mitiga o revierte el antagonismo D2. Cuál de las dos alternativas resulte vencedora –el antagonismo D2 o la estimulación dopaminérgica- dependerá del fármaco (para los antipsicóticos convencionales vence siempre el antagonismo D2), de la dosis (el antagonismo D2 es más fácil que venza en dosis altas de antipsicóticos atípicos) y de la vía del cerebro.
En la vía nigroestriada la TEP revela que un antipsicótico atípico bloquea entre el 70 y el 80% de los receptores D2. esto sitúa el umbral de bloqueo de los receptores D2 por debajo del nivel necesario para producir SEP en muchos pacientes.
La vía mesocortical y la farmacología de mejora de los signos negativos
A diferencia de la vía dopaminérgica nigroestriada, en la que predominan los receptores dopaminérgicos D2, en muchas partes de la corteza cerebral existe una preponderancia de los receptores 5HT2A sobre los receptores D2. Así, en la vía dopaminérgica mesocortical los antipsicóticos atípicos con propiedades ASD tienen un efecto más profundo en el bloqueo de los receptores corticales 5HT2A, densamente poblados – incrementando la liberación de dopamina-, que en el bloqueo de los receptores corticales D2, escasamente poblados. Esto da como resultado la unión de una considerable cantidad de antagonista 5HT2A y también una considerable liberación de dopamina, pero un menor antagonismo D2 en esa parte del cerebro. Resultado: la liberación de dopamina vence de nuevo sobre el bloqueo de la dopamina en el “tira y afloja” mesocortical. En la TEP se confirman estos resultados.
Recuérdese que se ha planteado la hipótesis de que el déficit de dopamina en la vía dopaminérgica mesocortical es una de las causas que contribuyen a los síntomas negativos de la esquizofrenia. Así, la naturaleza del antagonismo serotoninérgico-dopaminérgico en la vía dopaminérgica mesocortical ha ayudado a los antipsicóticos atípicos a resolver el dilema de cómo incrementar el teórico déficit de dopamina en esta vía para tratar los síntomas negativos y, no obstante, reducir a la vez la dopamina teóricamente hiperactiva en la vía dopaminérgica mesolímbica para tratar los síntomas positivos.
La vía tuberoinfundibular y la farmacología de reducción de la hiperprolactinemia
La dopamina inhibe la liberación de prolactina al estimular a los receptores D2, mientras que la serotonina favorece la liberación de prolactina al estimular a los receptores 5HT2A.
Así pues, cuando los receptores D2 son bloqueados por un antipsicótico convencional, la dopamina ya no puede inhibir la liberación de prolactina, de modo que los niveles de ésta se incrementan. Sin embargo, en el caso de un antipsicótico atípico, simultáneamente se da la inhibición de los receptores 5HT2A, de modo que la serotonina ya no puede estimular la liberación de prolactina. Esto tiende a mitigar la hiperprolactinemia del bloqueo de los receptores D2.
La vía mesolímbica y la farmacología de mejora de los síntomas positivos
Afortunadamente, el antagonismo 5HT2A revierte el antagonismo D2 en el sistema mesolímbico. Si el antagonismo 5HT2A revierte, al menos en parte, los efectos del antagonismo D2 en varias vías dopaminérgicas, entonces ¿por qué no revierte las acciones antipsicóticas del bloqueo D2 en la vía dopaminérgica mesolímbica? Evidentemente, el antagonismo por parte de la serotonina sobre los efectos de la dopamina en esta vía no es lo bastante fuerte como para causar la reversión de los receptores D2 por parte de los antipsicóticos atípicos o para mitigar las acciones de éstos sobre los síntomas positivos de la psicosis.
Resumen de las acciones de los antipsicóticos atípicos como clase
En el caso de los antipsicóticos convencionales el bloqueo de la dopamina vence el “tira y afloja” en todas las vías dopaminérgicas, dando como resultado acciones antipsicóticas sobre los síntomas positivos, pero al precio del empeoramiento –o, al menos, de la falta de mejora- de los síntomas negativos, y de la producción de SEP, discinesia tardía e hiperprolactinemia.
Por su parte, parece ser que los antipsicóticos atípicos permiten que el bloqueo de la dopamina venza a la liberación de dopamina en el “tira y afloja” allí donde debe vencer para tratar los perturbadores síntomas positivos, a saber, en la vía dopaminérgica mesolímbica; pero a la vez ocurre todo lo contrario en la vía dopaminérgica mesocortical, puesto que en dicha área cerebral la liberación de dopamina vence al bloqueo de la misma, y en consecuencia, mejoran los síntomas negativos. Y por si esto fuera poco, durante la administración de antipsicóticos atípicos la liberación de dopamina vence al bloqueo tanto en la vía dopaminérgica nigroestriada como en la tuberoinfundibular, en la medida suficiente como para reducir los SEP además de la hiperprolactinemia, produciendo en gran parte la eliminación de esos efectos secundarios indeseables.
Antipsicóticos atípicos: ¿varios fármacos únicos, o una clase integrada de varios fármacos?
Algunos ASD no poseen las propiedades clínicas atípicas de los cinco antipsicóticos atípicos (clozapina, risperidona, olanzapina, quetiapina y ziprasidona). Además cuando se administran en dosis altas, algunos ASD empiezan a perder sus propiedades atípicas. Por lo tanto hay que considerar otros factores farmacológicos y clínicos para poder comprender plenamente los diversos antipsicóticos actualmente considerados atípicos. Por otra parte, no hay dos agentes que tengan propiedades exactamente idénticas, incluyendo múltiples acciones farmacológicas en los subtipos de receptores serotoninérgicos y dopaminérgicos, además de las acciones ASD (p.e. D1, D3 y D4, 5HT1A, 5HT1D, 5HT2C, 5HT3, 5HT6 y 5HT7), y múltiples acciones farmacológicas en otros neurotransmisores (como los receptores noradrenérgicos alfa 1 y alfa 2, los receptores colinérgicos muscarínicos y los receptores de histamina H1, además de las bombas de recaptación tanto de serotonina como de norepinefrina).
Entre la propiedades farmacológicas favorables de los antipsicóticos atípicos se encuentran:
Mejora de síntomas negativos en pacientes esquizofrénicos
No causar un incremento en los niveles de prolactina
Mejora de los síntomas positivos
Mejora del estado de ánimo y reducción del suicidio, no sólo en pacientes esquizofrénicos sino en pacientes bipolares en las fases maníaca, mixta y depresiva de su enfermedad
Entre las propiedades clínicas adicionales desfavorables de los antipsicóticos atípicos se puede incluir:
Ganancia de peso
Sedación
Ataques convulsivos
Agranulocitosis
Cada uno de los principales antipsicóticos atípicos difiere de los demás en el grado en que se han podido establecer esas diversas características clínicas favorables y desfavorables. Por otra parte, los pacientes individuales pueden presentar respuestas muy distintas de la respuesta media predicha a partir de los resultados colectivos de los ensayos clínicos, así como respuestas muy distintas entre agentes.
Aunque todavía no está claro por qué los diversos antipsicóticos atípicos difieren entre sí, lo más probable es que la respuesta se halle en las propiedades farmacológicas, distintas del antagonismo 5HT2A y D2, que no tienen en común.
La idea de la sinergia entre múltiples mecanismos farmacológicos constituye también la base lógica de la combinación de fármacos de distintas acciones terapéuticas en pacientes que no responden a los diversos antidepresivos con mecanismos únicos. ¿Es posible que ocurra esto mismo con los pacientes psicóticos? Actualmente, el mejor antipsicótico atípico para un paciente individual se suele descubrir por ensayo y error.
Clozapina
La clozapina se considera el prototipo de los antipsicóticos atípicos, ya que fue el primero en el que se observó que tenía muy pocos efectos secundarios extrapiramidales, cuando no ninguno, no causaba discinesia tardía y no elevaba los niveles de prolactina. Aunque es un antagonista 5HT2A y D2, la clozapina también posee uno de los más complejos perfiles farmacológicos de la psicofarmacología, y no digamos entre los antipsicóticos atípicos.
Ocasionalmente los pacientes pueden experimentar un “despertar” (en el sentido de Oliver Sachs), caracterizado por el retorno a un nivel casi normal de funcionamiento cognitivo, interpersonal y profesional, y no sólo una mejora significativa de los síntomas de la psicosis, por desgracia se trata de un acontecimiento bastante raro.
Por otra parte, la clozapina es también el único fármaco antipsicótico asociado al riesgo de una complicación peligrosa, y puede que fatal, llamada agranulocitosis, que se da entre el 0,5 y el 2% de los pacientes. Entraña también un mayor riesgo de ataques convulsivos, especialmente en dosis elevadas.
Puede resultar muy sedante y se asocia al mayor grado de ganancia de peso entre todos los antipsicóticos.
En vista de la proporción de riesgos / beneficios de la clozapina, en general no se considera a ésta un agente de primera línea para el tratamiento de la psicosis, sino una opción a tener en cuenta cuando han fallado otros fármacos. Resulta especialmente útil para sofocar la violencia y la agresión en pacientes difíciles, puede reducir los índices de suicidio en la esquizofrenia, y puede reducir también la gravedad de la discinesia tardía, especialmente en períodos largos de tratamiento.
Risperidona
Este agente posee una estructura química distinta y un perfil farmacológico considerablemente más simple que el de la clozapina.
Se usa preferentemente en la esquizofrenia (en dosis moderadas), en los pacientes ancianos con psicosis, agitación y trastornos conductuales asociados con demencia, y en los niños y adolescentes con trastornos psicóticos. Los estudios actualmente en curso sugieren que puede mejorar el funcionamiento cognitivo no sólo en la esquizofrenia sino en el Alzheimer, y mejora el estado de ánimo en la esquizofrenia y en las fases tanto maníaca como depresiva del trastorno bipolar.
La risperidona resulta especialmente atípica en dosis bajas, pero en dosis elevadas puede volverse más “convencional” y si la dosis es alta puede darse SEP. Aunque es un ASD, por razones que no están claras eleva los niveles de prolactina, incluso en dosis bajas. Se produce una menor ganancia de peso que con otros agentes antipsicóticos atípicos, debido quizá a que la risperidona no bloquea los receptores histamínicos H1, aunque para algunos pacientes sigue siendo un problema.
Olanzapina
Aunque la olanzapina tiene una estructura química afín a la de la clozapina, es más potente que ésta y posee características farmacológicas y clínicas diferenciales, no sólo en relación a la clozapina, sino también en comparación con la risperidona.
La olanzapina es atípica en que generalmente carece de SEP, incluso con dosis altas. Tiende a utilizarse en algunos de los casos más difíciles de esquizofrenia, trastorno bipolar y otros tipos de psicosis en los que se desea un buen control de la psicosis sin que se produzca SEP, pero a la vez, se requiere un tratamiento agresivo. Por otra parte, este tratamiento puede resultar muy caro.
Puede resultar algo sedante, se asocia a la ganancia de peso, no suele elevar los niveles de prolactina y los estudios sugieren una muy baja incidencia de discinesia tardía con su uso a largo plazo.
Es sumamente eficaz en los síntomas positivos de la esquizofrenia y también mejora sus síntomas negativos. Mejora el estado de ánimo, tanto en la esquizofrenia como en las fases maníacas y depresivas del trastorno bipolar. Algunos estudios sugieren que la olanzapina puede mejorar el funcionamiento cognitivo en la esquizofrenia y la demencia.
Quetiapina
Presenta varias características farmacológicas y clínicas diferenciales con respecto a la clozapina, risperidona y olanzapina. La quetiapina es muy atípica en el hecho de que no causa SEP a ninguna dosis, ni tampoco eleva los niveles de prolactina. Tiende a ser el antipsicótico preferido por los pacientes con enfermedad de Parkinson y psicosis. También resulta útil en la esquizofrenia y el trastorno bipolar.
La quetiapina puede causar cierta ganancia de peso, ya que bloquea los receptores histamínicos H1 y ha mostrado una inhibición específica de la biosíntesis del colesterol en el cristalino de algunas especies animales, causando cataratas.
Es sumamente eficaz en los síntomas positivos de la esquizofrenia y también mejora sus síntomas negativos. Mejora el estado de ánimo, tanto en la esquizofrenia como en las fases maníacas y depresivas del trastorno bipolar. Algunos estudios sugieren que la quetiapina puede mejorar el funcionamiento cognitivo en la esquizofrenia y la demencia.
Ziprasidona
Presenta una estructura química novedosa y un perfil farmacológico también bastante novedoso en comparación con los demás antipsicóticos atípicos.
La ziprasidona parece ser atípica en el hecho de que presenta pocos SEP y produce poco o ningún aumento de los niveles de prolactina. Su principal característica diferencial dentro de su clase es que parece mostrar muy poca tendencia a causar ganancia de peso, debido a que carece de propiedades antihistamínicas. Asimismo, es el único antipsicótico atípico que es antagonista 5HT1D y 5HT1A, y también inhibe la recaptación de serotonina como de norepinefrina. Cabría esperar que estas últimas acciones farmacológicas fueran tanto proserotoninérgicas como pronoradrenérgicas, lo que podría contribuir al comportamiento favorable de la ziprasidona en lo que se refiere al peso, pero también predeciría sus acciones antidepresivas y ansiolíticas.
Es sumamente eficaz en los síntomas positivos de la esquizofrenia y también mejora sus síntomas negativos. Algunos estudios sugieren que la ziprasidona puede mejorar el funcionamiento cognitivo en la esquizofrenia y la demencia.
Los antipsicóticos atípicos en la práctica clínica
Los antipsicóticos atípicos siguen siendo relativamente nuevos, en particular algunos de los miembros de esta clase. La información sobre nuevos fármacos está disponible en un primer momento a partir de pruebas clínicas y luego se modifica en función de las observaciones de la práctica clínica, y los antipsicóticos atípicos no son una excepción. Algunos hallazgos de la práctica clínica han confirmado ya los de las pruebas clínicas para los tres antipsicóticos atípicos actualmente comercializados, es decir, la risperidona, la olanzapina y la quetiapina. Se sabe menos de la ziprasidona, el miembro más reciente de este grupo.
Hay cuatro hallazgos importantes:
No cabe duda de que los antipsicóticos atípicos producen mucho menos SEP que los antipsicóticos convencionales, es decir, hacen lo que se anuncia y lo que se predice farmacológicamente que harán.
Reducen los síntomas negativos de la esquizofrenia mejor que los convencionales, pero esto puede deberse tanto a que no empeoran las cosas como a que reduzcan los síntomas negativos.
Reducen los síntomas afectivos en la esquizofrenia y en los trastornos relacionados como la depresión resistente al tratamiento y en el trastorno bipolar.
Pueden reducir los síntomas cognitivos en la esquizofrenia y en el Alzheimer.
Por otra parte, no todo lo que sugieren los ensayos clínicos controlados, realizados con poblaciones limitadas de pacientes sometidos a estudios en situaciones ideales, resulta aplicable en el mundo real de la práctica clínica.
Efectos diversos en distintos pacientes.
Las dosis óptimas sugeridas por los ensayos clínicos a menudo no coinciden con las dosis óptimas utilizadas en la práctica clínica.
Es posible que los antipsicóticos atípicos no funcionen tan rápido como los convencionales.
Casi todos los estudios son comparaciones directas de monoterapias y/o placebos, y en la práctica clínica muchos pacientes reciben dos fármacos psicóticos.
Uso de los antipsicóticos atípicos para los síntomas positivos de la esquizofrenia y los trastornos relacionados
Aunque la utilidad de los antipsicóticos atípicos está mejor documentada para los síntomas positivos de la esquizofrenia, numerosos estudios están revelando su utilidad en el tratamiento de los síntomas positivos asociados a varios trastornos. De hecho, en muchos países las actuales pautas de tratamiento han evolucionado de modo que los antipsicóticos atípicos han reemplazado en gran medida a los convencionales para el tratamiento de los síntomas psicóticos positivos excepto en unas pocas situaciones clínicas específicas.
Antipsicóticos convencionales: entorno especialmente agudo en un paciente que no coopera (posología intramuscular- acción rápida, más una benzodiacepina).
Antipsicóticos convencionales: pacientes que no cumplen las pautas de tratamiento (inyecciones mensuales de un antipsicótico depot)
Todavía no existe ningún antipsicótico atípico disponible para su administración depot. La mayoría de los clínicos elige de entre “la farmacia de los síntomas positivos” aquél que sea más adecuado a su paciente.
Polifarmacia de los síntomas positivos
En caso de emergencia: BZ+D2 intramuscular
1a línea: ASD
No cumplimiento: D2 intramuscular
2a línea: D2 + Clozapina
3a Línea: polifarmacia + combos
Uso de los antipsicóticos atípicos para los trastornos del estado de ánimo en la esquizofrenia y los trastornos relacionados
Los profundos efectos estabilizadores del estado de ánimo de los fármacos antipsicóticos atípicos se observaron una vez documentados sus efectos antipsicóticos. Dichos efectos en el estado de ánimo parecen ser bastante independientes de sus efectos en los síntomas positivos de la psicosis. Lo más espectacular es el impresionante efecto que los antipsicóticos atípicos están demostrando tener en el tratamiento bipolar.
Farmacia de los síntomas afectivos
1a línea: ASD. Síntomas psicóticos del trastorno bipolar, estabilizador de los estados de ánimo maníacos, mixtos, de ciclos rápidos y resistentes al tratamiento en pacientes bipolares.
Reducción del índice de suicidio: ASD, en pacientes esquizofrénicos y bipolares.
Mejora del estado de ánimo, la ansiedad e, incluso, la depresión: ASD, en varios trastornos además de la depresión mayor.
2a línea: ASD+ISRS+Clozapina. Los antipsicóticos atípicos se emplean como coadyuvantes de los antidepresivos de los casos resistentes al tratamiento de depresión unipolar no psicótica.
Uso de los antipsicóticos atípicos para los síntomas cognitivos de la esquizofrenia y otros trastornos relacionados
La gravedad de los síntomas cognitivos se corresponde con el pronóstico a largo plazo de la esquizofrenia.
Los síntomas cognitivos constituyen claramente una dimensión de la psicopatología que afecta a muchos trastornos en psiquiatría y neurología. Los ASD pueden mejorar la cognición de estos trastornos, y lo hacen independientemente de su capacidad para reducir los síntomas positivos de la psicosis.
En la esquizofrenia puede haber mejoras en la fluidez verbal, el aprendizaje en serie y el funcionamiento ejecutivo.
En el Alzheimer puede haber mejoras en la memoria y en el comportamiento, que pueden resultar aditivas, o incluso sinérgicas, con la mejora obtenida por medio de un tratamiento concomitante con otros tipos de potenciadores cognitivos, como los inhibidores de la colinesterasa (ICE).
Uso de los antipsicóticos atípicos para los síntomas negativos de la esquizofrenia
Se cree que los síntomas negativos de la esquizofrenia constituyen un rasgo particularmente único, aunque ciertos aspectos de dichos síntomas no son exclusivos de la propia esquizofrenia. Cualquier mejora en los síntomas negativos que se puede obtener por medio del tratamiento con antipsicóticos atípicos resulta de gran importancia, ya que el resultado a largo plazo de la esquizofrenia se halla más estrechamente relacionado con la gravedad de los síntomas negativos que con la de los positivos.
Sin embargo, ya está claro que harán falta efectos del tratamiento significativamente más sólidos que los ofrecidos por los antipsicóticos atípicos se han de eliminar dichos síntomas en la mayoría de los pacientes esquizofrénicos.
Hay dos métodos para mejorar los síntomas a corto plazo:
Los síntomas negativos secundarios a los antipsicóticos convencionales se pueden reducir inmediatamente sustituyéndolos por antipsicóticos atípicos.
Los antipsicóticos atípicos realmente mejoran los síntomas negativos. En la olanzapina y la risperidona ya se ha documentado una mayor mejoría de los síntomas negativos que en los convencionales. Para la quetiapina y la ziprasidona se ha documentado una mayor mejoría que con los placebos.
Uso de los antipsicóticos atípicos para tratar la hostilidad, la agresión y el escaso control de impulsos en la esquizofrenia y los trastornos relacionados
Esto puede adoptar la forma de intentos de suicidio, automutilación, escaso control de impulsos, abuso de drogas, agresión verbal, agresión física y/o conducta amenazadora, y es posible que no se correlacione directamente con los síntomas positivos. En un entorno forense esto puede llegar a ser problemático.
Obviamente, esta dimensión de la psicopatología abarca una amplia franja de trastornos psiquiátricos, y no está necesariamente asociada a la psicosis. Tanto los antipsicóticos convencionales como los atípicos reducen dichos síntomas, pero existen muchos más estudios sobre la hostilidad y la agresión en enfermedades psicóticas que en las no psicóticas.
Farmacia de los síntomas agresivos
En caso de emergencia: BZ + D2 intramuscular
1a Línea: ASD
2a Línea: Clozapina + BZ + D2
Polifarmacia antipsicótica y gestión de la resistencia al tratamiento de la esquizofrenia
Los pacientes esquizofrénicos normalmente responden al tratamiento con un solo fármaco antipsicótico, sea convencional o atípico, mejorando sus síntomas positivos al menos en un 30 ó 40% al cabo de un mes o dos de tratamiento. Sin embargo, si no se observa un efecto de esta magnitud, la mayoría de los clínicos optan por otro fármaco antipsicótico atípico. Cuando se pasa de uno a otro, con frecuencia suele ser prudente utilizar la sustitución gradual, es decir, disminuir la dosis del primer fármaco a la vez que se aumenta la del segundo, donde es posible quedar atrapado. Dicho de otro modo, mientras se realiza el cambio, el paciente puede experimentar una mejora en plena sustitución y el clínico decide continuar con ambos fármacos, en lugar de completar el cambio.
Este tipo de polifarmacia no está justificado y es inaceptable. Sólo después de varios fracasos con monoterapias secuenciales, incluyendo la clozapina y los antipsicóticos convencionales, se debería administrar la polifarmacia con dos antipsicóticos a largo plazo (casos graves – brotes de agresividad).
La utilización de dos fármacos antipsicóticos parece ser uno de los fenómenos más practicados (una cuarta parte de los pacientes ambulatorios y la mitad de los ingresados) y menos investigados de la psicofarmacología clínica.